合成生物學(xué)是一個以科學(xué)為基礎(chǔ),設(shè)計為驅(qū)動的新興領(lǐng)域。通過分子水平的設(shè)計創(chuàng)造新的產(chǎn)品及解決方案或優(yōu)化原有工藝,增加珍稀原材料的可用性、降低生產(chǎn)成本、同時,減少對資源的消耗、環(huán)境的破壞,生產(chǎn)可持續(xù)發(fā)展的產(chǎn)品。合成生物學(xué)的技術(shù)邏輯是設(shè)計—構(gòu)建—測試—學(xué)習(xí)(DBTL),制造技術(shù)是合成生物學(xué)的核心;大數(shù)據(jù)、算法開發(fā)以及“讀”-“寫”-“編”的融合是合成生物學(xué)的引擎。合成生物學(xué)幾乎可以為任何行業(yè)的新品開發(fā)和過程改良提供新的思路和方法,先進(jìn)制造與算法的結(jié)合促進(jìn)產(chǎn)品在垂直領(lǐng)域的爆發(fā)即是合成生物學(xué)的核心思維。
合成生物學(xué)催生了生物經(jīng)濟(jì)。根據(jù)Maximize Market Research的數(shù)據(jù),2020年全球合成生物學(xué)市場已達(dá)到75億美元,預(yù)計至2027年將超過380億美元,年復(fù)合年增長率(CAGR)為26.5%。合成生物學(xué)在未來10-20年將解決全球45%的疾病和60%的人類物質(zhì)需求。基于合成生物學(xué)技術(shù)革命的生物智造將在2030-2040年間每年為全球帶來2-4萬億美元的直接經(jīng)濟(jì)效益。農(nóng)業(yè)、食品、醫(yī)療、健康、能源、材料、化工、通訊、環(huán)境等行業(yè)均會產(chǎn)生顛覆性變革。
合成生物學(xué)在生物醫(yī)藥領(lǐng)域
合成生物學(xué)在生物醫(yī)藥領(lǐng)域的發(fā)展受益于生物技術(shù)及基因工程的發(fā)展,如全基因組測序、轉(zhuǎn)錄組測序等多組學(xué)測序技術(shù),提高了研究人員對基因調(diào)控網(wǎng)絡(luò)的認(rèn)識;大規(guī)模基因合成及編輯技術(shù)使得科學(xué)家們能夠快速迭代多基因設(shè)計與功能驗(yàn)證;定向進(jìn)化及分子建模等技術(shù)實(shí)現(xiàn)了合成生物學(xué)家們對于設(shè)計驅(qū)動核酸、蛋白質(zhì)工程以選擇和創(chuàng)建具有功能性生物分子和系統(tǒng)的創(chuàng)想。合理設(shè)計與不同技術(shù)的結(jié)合,極大推動了生物醫(yī)藥在疾病的診斷、預(yù)防及治療中的發(fā)展和臨床轉(zhuǎn)化。
診斷
基于合成生物學(xué)技術(shù)已經(jīng)開發(fā)出幾種創(chuàng)新型診斷方法,如基于紙質(zhì)的腳踏開關(guān)RNA分子和基于CRISPR/Cas蛋白的診斷。腳踏開關(guān)是一種原核生物核糖調(diào)節(jié)劑,可在檢測目標(biāo)核酸后驅(qū)動蛋白質(zhì)表達(dá)。常規(guī)狀態(tài)下,莖環(huán)結(jié)構(gòu)可以將核糖體結(jié)合序列(RBS)和腳踏開關(guān)的AUG分離,防止報告基因翻譯。工作狀態(tài)下,RNA與目標(biāo)序列結(jié)合后,RBS和AUG被釋放并啟動下游翻譯。下游翻譯的可以是任何蛋白質(zhì),所以該系統(tǒng)很容易適應(yīng)熒光、生物發(fā)光、比色、生物電輸出等方式。同時,這款檢測器可以通過冷凍干燥的方式固定到紙質(zhì)基質(zhì)上,即使在室溫下長時間儲存也能保持活性。研究人員利用紙質(zhì)無細(xì)胞表達(dá)系統(tǒng)、等溫核酸擴(kuò)增和腳踏開關(guān)的組合為診斷基礎(chǔ)設(shè)施嚴(yán)重短缺的地區(qū)提供了一個適應(yīng)性強(qiáng)、靈敏且穩(wěn)定的診斷平臺,目前已成功應(yīng)用于寨卡病毒診斷。基于鏈切割的CRISPR診斷提供了一種靈敏度更高和反應(yīng)更簡單的方法。CRISPR診斷結(jié)合了RPA擴(kuò)增、Cas12a/Cas13a檢測、DNA/RNA探針切割幾個過程,可實(shí)現(xiàn)對疾病的高性能即時檢測。如其中兩種基于CRISPR的技術(shù)—SHERLOCK和DETECTR,已被FDA授予EUA,用于在人類臨床樣本中檢測SARS-CoV-2。
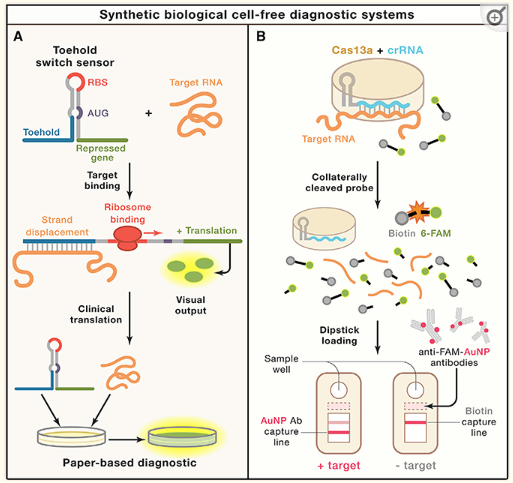
圖1基于合成生物學(xué)的無細(xì)胞診斷(Cell. 2021 Feb 18; 184(4): 881–898)
預(yù)防
疫苗是用于降低多種疾病的發(fā)病率和死亡率的有效手段。疫苗的方法可以分為滅活疫苗、減毒疫苗、重組蛋白疫苗、腺病毒載體疫苗、核酸疫苗等。合成生物學(xué)的發(fā)展,使得疫苗設(shè)計和生產(chǎn)取得重大進(jìn)展。a.通過大規(guī)模同義突變重新設(shè)計整個病毒基因組以獲得減毒毒株。該方法利用了密碼子的簡并性,合成生物學(xué)家們有目的地使用非代表性密碼子來減少病毒蛋白的產(chǎn)生,案例有脊髓灰質(zhì)炎疫苗、減毒流感病毒疫苗、呼吸道合胞病毒疫苗和登革熱病毒疫苗等。b.設(shè)計核酸疫苗。核酸疫苗是通過將編碼病毒成分的DNA或RNA引入細(xì)胞,然后在自然感染過程中誘導(dǎo)機(jī)體產(chǎn)生細(xì)胞和體液免疫,其優(yōu)勢在于設(shè)計速度和生產(chǎn)流程簡單、靶向表位豐富。以RNA疫苗為例,合成生物學(xué)家通過密碼子優(yōu)化、使用修飾核苷、改進(jìn)遞送系統(tǒng)等方式提高了mRNA在體內(nèi)穩(wěn)定性和翻譯效率。
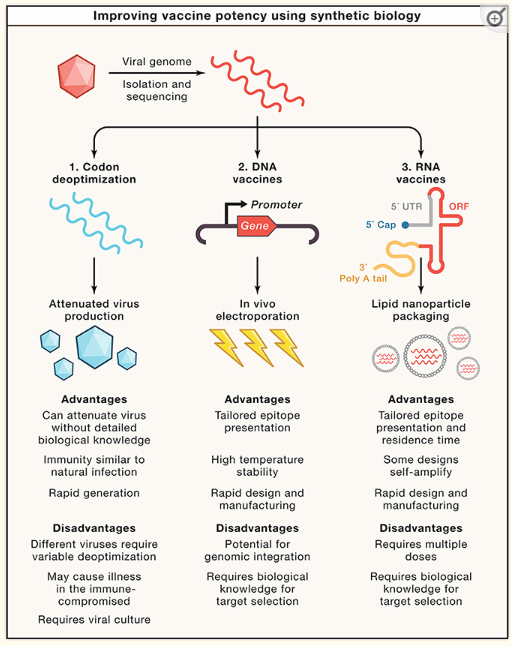
圖2合成生物學(xué)與疫苗設(shè)計(Cell. 2021 Feb 18; 184(4): 881–898)
治療
合成生物學(xué)的治療潛力在哺乳動物疾病治療中的應(yīng)用越來越普遍,代表著其發(fā)現(xiàn)新藥物靶點(diǎn)和設(shè)計新的疾病治療策略具有巨大潛力。在藥物靶點(diǎn)方篩選面,CRISPR系統(tǒng)正在用于哺乳動物疾病治療的藥物靶點(diǎn)篩選和鑒定。如將合成的CRISPR sgRNA文庫進(jìn)行細(xì)胞轉(zhuǎn)染,經(jīng)過藥物處理、表型篩選、NGS測序分析表達(dá)差異基因來篩選和鑒定藥物靶點(diǎn)。在疾病治療策略方面,基因治療和細(xì)胞免疫療法是兩種發(fā)展較快的領(lǐng)域。如嵌合抗原受體(CAR)T細(xì)胞療法,已成為幾種血癌的突破性、臨床批準(zhǔn)的治療方法。CAR由一個外部單鏈可變片段(scFv)、一個CD8α跨膜結(jié)構(gòu)域、一個來自T細(xì)胞受體的細(xì)胞內(nèi)CD3z結(jié)構(gòu)域和一個共刺激結(jié)構(gòu)域(CD28或4-1BB)組成。當(dāng)靶抗原與scFv結(jié)合時,可激活刺激域和共刺激域以促進(jìn)T細(xì)胞增殖和靶細(xì)胞殺傷。合成生物學(xué)對其功能進(jìn)行精確設(shè)計和控制可進(jìn)一步提高其特異性和細(xì)胞殺傷能力。
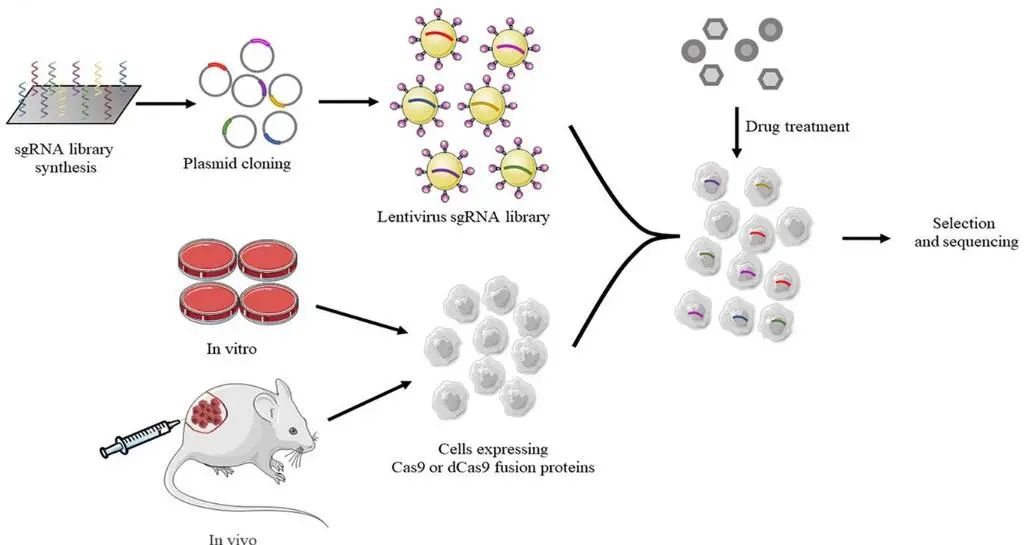
圖3 CRISPR系統(tǒng)應(yīng)用于藥物靶點(diǎn)篩選(Front Pharmacol. 2020; 11: 119)
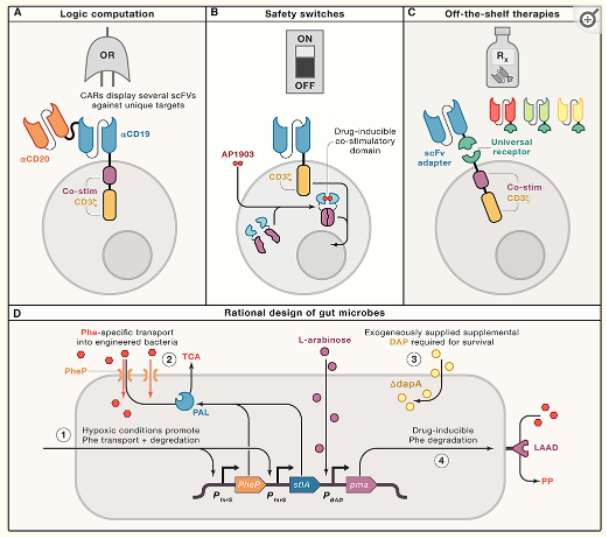
圖4利用合成生物學(xué)擴(kuò)展細(xì)胞療法(Cell. 2021 Feb 18; 184(4): 881–898)
合成生物學(xué)在工業(yè)領(lǐng)域
合成生物學(xué)和工業(yè)生物技術(shù)被認(rèn)為是生物經(jīng)濟(jì)發(fā)展的關(guān)鍵平臺,這兩種技術(shù)的結(jié)合對于支持可持續(xù)發(fā)展并實(shí)現(xiàn)技術(shù)驅(qū)動生物經(jīng)濟(jì)的戰(zhàn)略利益非常重要。在未來,60%的工業(yè)產(chǎn)品都可以通過生物技術(shù)進(jìn)行制造。在工業(yè)領(lǐng)域,合成生物學(xué)通常通過設(shè)計微生物、優(yōu)化酶以及大規(guī)模發(fā)酵來生產(chǎn)可替代大宗化學(xué)品和特殊化學(xué)品的生物產(chǎn)品。設(shè)計—構(gòu)建—測試—學(xué)習(xí)(DBTL)的循環(huán)構(gòu)成了發(fā)現(xiàn)和優(yōu)化目標(biāo)系統(tǒng)的基本特征。
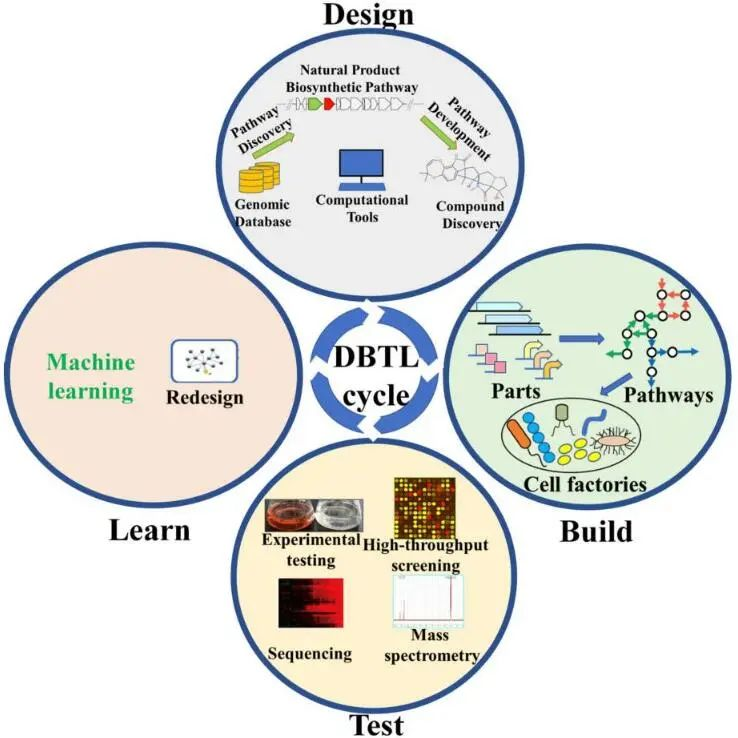
圖5設(shè)計—構(gòu)建—測試—學(xué)習(xí)(DBTL)的循環(huán)(Metabolites. 2021 Nov; 11(11): 785)
天然產(chǎn)物及化學(xué)品
植物天然產(chǎn)物因其可用作香精、香料和藥物而成為特別重要的開發(fā)目標(biāo),但由于天然產(chǎn)物的結(jié)構(gòu)復(fù)雜,用化學(xué)合成的方法也面臨過程復(fù)雜、能耗多等問題。于是,生物合成為天然產(chǎn)物和其他化學(xué)品的生產(chǎn)提供了新的思路和機(jī)會。如合成生物學(xué)家通過微生物設(shè)計,發(fā)酵獲得天然香草醛,提高了稀缺原材料的產(chǎn)量和可用性。以及通過特殊設(shè)計的酵母菌株生產(chǎn)膠原蛋白,可賦予皮革更優(yōu)秀的強(qiáng)度和彈性。經(jīng)過提純、鞣制等一系列操作,生產(chǎn)出的膠原蛋白就變得幾乎和皮革一樣。
農(nóng)業(yè)與食品
在農(nóng)業(yè)中,研究人員設(shè)計了一款微生物,可以使玉米、小麥和水稻等作物更有效地利用肥料,減少氮肥使用數(shù)量,同時此微生物還可以保護(hù)植物免受病蟲害的侵害。以及在合成肉行業(yè),研究人員從幾個品種的雞、牛、鴨等動物中提取干細(xì)胞,為它們提供氨基酸、碳水化合物、礦物質(zhì)、脂肪和維生素等營養(yǎng)物質(zhì),并使用生物反應(yīng)器加速這些細(xì)胞的生長,從而大規(guī)模生產(chǎn)合成肉。或者使用小麥、馬鈴薯蛋白、向日葵、椰子油、甲基纖維素、食用淀粉以及實(shí)驗(yàn)室設(shè)計的非肉類血紅素分子來制作牛肉漢堡肉餅。這些途徑不僅減輕了飼養(yǎng)動物對土地、水等自然資源的占用,對環(huán)境的影響及避免了潛在的生物污染風(fēng)險。
紡織品
在紡織行業(yè),原來生產(chǎn)一噸染料需要使用1000立方米的水、100噸重石油化合物、10噸有毒和腐蝕性化學(xué)品,以及至少200兆焦/噸的能源。對環(huán)境的影響巨大。在新興初創(chuàng)企業(yè)中,合成生物學(xué)家更傾向于使用酶將可再生資源中的碳轉(zhuǎn)化為可用于生產(chǎn)紡織染料的分子,從而減少對能源的消耗和副產(chǎn)品的產(chǎn)生。這一系列酶是通過改造微生物產(chǎn)生的,不僅可以將碳轉(zhuǎn)化為染料或顏料,還可以通過交換酶和優(yōu)化代謝工程過程產(chǎn)生多種顏色。又如,用來制造地毯、服裝、汽車內(nèi)飾、工程塑料和食品包裝的尼龍6,通過工藝優(yōu)化,研究人員引入一種特殊設(shè)計的微生物,可將植物中的糖(而非石油)發(fā)酵成尼龍6生產(chǎn)中的關(guān)鍵中間體。不僅解決了對環(huán)境的污染問題,還有望將生物尼龍生產(chǎn)能力提高幾十倍。
生物能源
在采礦業(yè),礦業(yè)公司正在試驗(yàn)生物浸出和生物氧化,即利用微生物從開采的礦石中提取銅、鈾和金等金屬。此種方法可確保提取率超過90%,且整個過程會降低成本和能耗,對景觀的破壞也較小。此外,還有一些化學(xué)品的生產(chǎn)過度依賴石化產(chǎn)品、并且,其衍生物或生產(chǎn)過程會產(chǎn)生大量有害化學(xué)品及廢物,如在塑料、彈性纖維(如氨綸)和聚氨酯的制造中用作溶劑的BDO(1,4-丁二醇)、用于制造合成橡膠(聚異戊二烯)的合成生物單體等。合成生物學(xué)家們正在嘗試使用可再生碳水化合物原材料和特殊設(shè)計的微生物來進(jìn)行生物替代品的生產(chǎn),普及后,年產(chǎn)量不僅會翻幾倍,二氧化碳的排放也會顯著減少。
泓迅生物與合成生物學(xué)
合成生物學(xué)的出現(xiàn)與其他顛覆性技術(shù)一樣,為企業(yè)的創(chuàng)新和改型提供了無數(shù)種可能性與挑戰(zhàn)。
合成生物學(xué)技術(shù)正走向成熟,無論來自何種行業(yè),每個企業(yè)都需要保持與時俱進(jìn)的思想、深度學(xué)習(xí)的能力,以及不斷進(jìn)行技術(shù)升級、組合、測試,思考未來商業(yè)模式,才有可能從容應(yīng)對這場顛覆性的變革。
泓迅生物自成立起,致力于成為合成生物學(xué)賦能技術(shù)領(lǐng)導(dǎo)者,立足自身完備的基因制造平臺與生物設(shè)計平臺,閉環(huán)DBTL技術(shù)需求,為合成生物學(xué)的發(fā)展提供有效的技術(shù)工具及解決方案。我們已為生命科學(xué)研究、合成生物學(xué)開發(fā)、抗體藥物篩選、疫苗研發(fā)、分子育種及DNA信息儲存等領(lǐng)域提供強(qiáng)有力的支持。未來,泓迅生物將一如既往地專注賦能能力,保持市場競爭力和可持續(xù)發(fā)展性。為合作伙伴的合成生物學(xué)技術(shù)開發(fā)添磚加瓦。
參考文獻(xiàn):
[1]Tan X, Letendre JH, Collins JJ, Wong WW. Synthetic biology in the clinic: engineering vaccines, diagnostics, and therapeutics. Cell. 2021;184(4):881-898. doi:10.1016/j.cell.2021.01.017
[2]Xie Y, Yang Y, He Y, et al. Synthetic Biology Speeds Up Drug Target Discovery. Front Pharmacol. 2020;11:119. Published 2020 Feb 26. doi:10.3389/fphar.2020.00119
[3]Wang J, Nielsen J, Liu Z. Synthetic Biology Advanced Natural Product Discovery. Metabolites. 2021;11(11):785. Published 2021 Nov 17. doi:10.3390/metabo11110785
[4]https://www.bcg.com/publications/2022/synthetic-biology-is-about-to-disrupt-your-industry
 Syno?C 引物合成
Syno?C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno?GS 基因合成
Syno?GS 基因合成 載體構(gòu)建
載體構(gòu)建 高通量及DNA文庫構(gòu)建
高通量及DNA文庫構(gòu)建 CRISPR基因編輯平臺
CRISPR基因編輯平臺 病毒包裝
病毒包裝 基因測序及分析
基因測序及分析 重組蛋白表達(dá)平臺
重組蛋白表達(dá)平臺 抗體工程平臺
抗體工程平臺 多肽服務(wù)
多肽服務(wù) 生物信息學(xué)分析與設(shè)計
生物信息學(xué)分析與設(shè)計 CRISPR文庫
CRISPR文庫 ProXpress蛋白快速檢測
ProXpress蛋白快速檢測 CRISPR 質(zhì)粒
CRISPR 質(zhì)粒





















